|
|
BMe Kutatói pályázat |
|
Oláh György Doktori Iskola
BME VBK, Lágy Anyagok Kutatócsoport, Fizikai Kémia és Anyagtudományi Tanszék
Témavezető: Dr. Szilágyi András
Redox hatásra gélesedő poliaminosavak
A kutatási téma néhány soros bemutatása
A mai gyógyszerformák legfontosabb feladata a hatóanyag pontos célba juttatása, mely lehetővé teszi a szükséges dózismennyiség csökkentését, ezzel az esetleges mellékhatások visszaszorítását. A hidrogélek nagy víztartalmú, polimer alapú anyagok, melyek kompatibilisek a szöveteinkkel és alkalmasak a bezárt hatóanyag szabályozott és célzott leadására. PhD munkám során olyan poliaminosav alapú hidrogéleket fejlesztettem, melyek reagálnak a fiziológiai paraméterek (pH és redox potenciál) megváltozására, és várhatóan alkalmazhatóak lesznek célzott rákterápiában, kihasználva a rákos és egészséges sejtek oxidációs állapotának eltérését.
A kutatóhely rövid bemutatása
A Lágy Anyagok Kutatócsoport várhatóan gyógyászati alkalmazással bíró, reszponzív polimer hidrogélek fejlesztésével foglalkozik. Korábban akrilát alapú géleket állítottunk elő, melyek tulajdonságait a környezetük paramétereivel szabályoztuk [1,2]. Az utóbbi néhány évben kutatásunk középpontjába a gyógyászati alkalmazások szempontjából ígéretes poliaminosavak kerültek [3].
A kutatás történetének, tágabb kontextusának bemutatása
A gélek háromdimenziós térhálós szerkezetek, melyek molekulákból, polimerekből vagy részecskékből épülnek fel, és a térhálót a funkciós csoportok közötti kölcsönhatások tartják össze [4]. Legfontosabb csoportjukat a polimer hidrogélek képezik, melyek nagy vízfelvételre képes, makromolekuláris rendszerek, és sok esetben reszponzív sajátságokkal rendelkeznek, azaz képesek kölcsönhatásba lépni környezetükkel [5]. A reszponzív hidrogélek az őket érő hatásokra egy meghatározott térfogati vagy egyéb válaszreakcióval reagálnak [6].
A reszponzív hidrogélek legismertebb képviselői a hőmérséklet-érzékeny polimerek [7]. Fontos azonban kiemelni, hogy a gyógyászati alkalmazásokkal kapcsolatos kihívásokat csak az úgynevezett multireszponzív hidrogélek tudják teljesíteni, melyek válaszreakciót mutatnak több, biológiai szempontból releváns környezeti hatásra is, például szénhidrát koncentrációra (glükóz koncentrációtól függő inzulin kibocsátás, 1. ábra) vagy egy adott enzim vérszintjére [8,9].
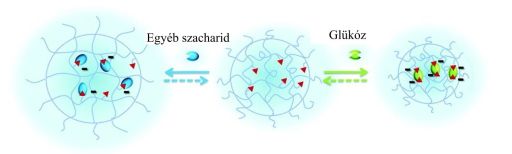
1. ábra A gél glükóz jelenlétében megváltoztatja a térfogatát és leadja a térhálóba zárt inzulin egy részét; a gél válaszreakciója szelektív, a szacharidok közül csak a glükóz jelenlétére reagál [9].
Az in situ (az alkalmazás helyén) képződő hidrogélek a műtéti beavatkozást a hagyományos gélekhez képest jóval egyszerűbbé teszik [10]. Példaként a hőmérséklet-érzékeny polimereket említjük, melyek fecskendővel bejuttathatóak a szervezetbe, és csak a testhőmérsékleten hozzák létre a gél szerkezetet. [11] (2. ábra). A hőmérséklet-érzékeny polimerek hátránya, hogy idő előtt gélesedhetnek (például az injektálás során fellépő súrlódási hő miatt), ami a fecskendő eltömődését okozhatja. Az enzimatikus vagy oxidáció hatására bekövetkező gélesedés megfelelő alternatíva lehet a szabályozottabb gélesedés megvalósítására. Az oxidatív gélesítés könnyen megvalósítható a szervezetben lejátszódó redox folyamatok analógiájára [12].
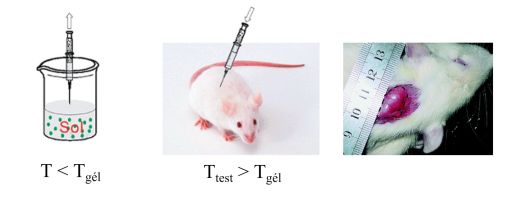
2. ábra A könnyen folyó polimer oldat (szol) injektálása, majd in situ gélesedése a szervezet kiválasztott pontján. A gélesedés ebben az esetben a kísérleti állat bőre alatt történt [11].
A kutatás célja, a megválaszolandó kérdések.
Célom a kutatócsoportban kutatott poliaminosavakból kiindulva olyan hidrogélek szintézise volt, melyek a környezet pH-jának vagy redox potenciáljának megváltozására jól definiált, jelentős válaszreakcióval reagálnak. A glutation (egy tiol csoportot tartalmazó peptid) által szabályozott, a szervezetben lejátszódód redox folyamatok mintájára a tiol-diszulfid átalakulást kívántam felhasználni a szintézis és a válaszreakció megvalósítása során. Elsődleges célom oxidáció hatására gélesedő polimer oldat előállítása volt, mely csak az injektálást követően hozza létre a gél szerkezetet [13]. A polimer előnyös tulajdonságai – kompatibilitás az emberi szövetekkel, biológiai lebonthatóság és a tiolcsoportok által biztosított adhézió – mind hozzájárulhatnak a tervezett formula sikeres gyógyászati alkalmazásához [14,15].
Módszerek
Kutatómunkám lényegi részét képezte a megfelelő válaszreakciót biztosító hidrogél megtervezése és szintézise. A poliaszparaginsav mint szintetikus polipeptid felhasználásával állítottam elő a polimert, melyre tiol oldalcsoportokat vittem fel kémiai reakcióban; a tiolcsoportok oxidáció hatására összekapcsolódhatnak (3. ábra).
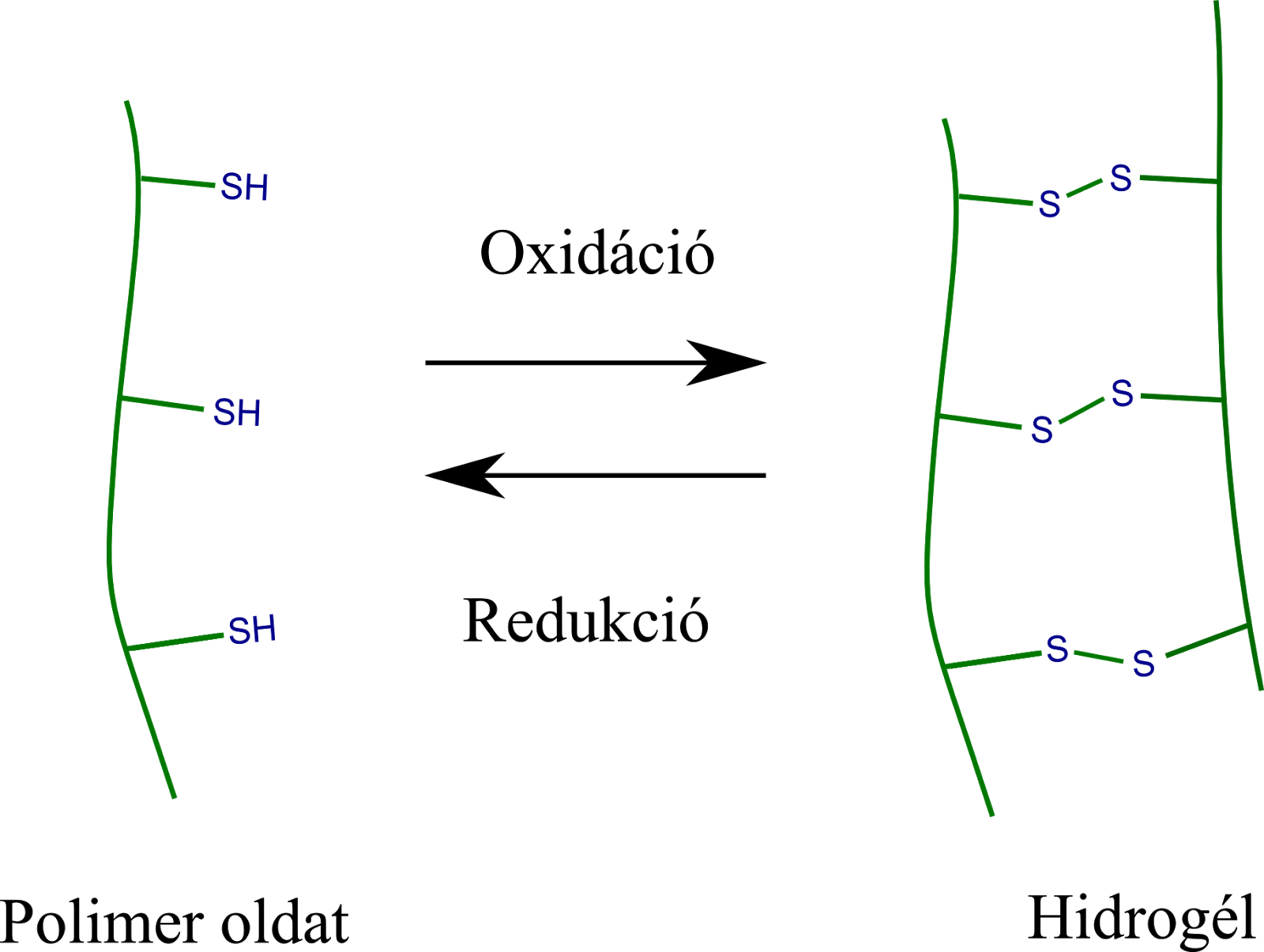
3. ábra Kémiai kapcsolás és a létrejövő diszulfid kötés bontása oxidáció és redukció hatására
A polimer kémiai szerkezetét különböző kémiai és spektroszkópiai módszerekkel tanulmányoztam, például mágneses magrezonancia és Raman mikroszkópia alkalmazásával. A tioltartalmú polimer oldatának oxidációjával hidrogéleket állítottam elő, és a gélesedés folyamatát szabad szemmel, valamint mechanikai mérésekkel (rugalmassági modulus mérése és reológia) vizsgáltam. Modell hatóanyag-molekulákat zártam be a mátrixba gélesedés során, és mértem a kioldódás sebességét a környezeti redox viszonyok függvényében, hogy megmutassam az előállított hidrogélek alkalmasságát redox hatással szabályozott hatóanyagi-leadó rendszerként.
Eddigi eredmények
Mágneses magrezonancia mérésekkel bizonyítottam a polimer szintézis sikerességét, és megmutattam, hogy a tiol csoportok koncentrációja szabályozható. Az előállított polimerek jól oldódnak vízben, és egy könnyen folyó oldatot kaptam. A polimer oldat oxidálószer hatására gélesedik a tiol csoportok között kialakuló kémiai kötésekből eredően (4. ábra) [GY1, GY2].

4. ábra A tioltartalmú poliaszparaginsav oxidáció hatására makroszkopikus hidrogéllé alakul (a gél szélessége mintegy 1 cm)
A polimer oldatok gélesedési folyamatát reológiai mérésekkel jellemeztem. A gélek merevsége egy széles koncentrációtartományon állandónak bizonyult, míg a gélesedési idő az összetétellel könnyen szabályozható (5. ábra). Ennek megfelelően, a polimer oldatból keletkező gél mechanikai tulajdonságai tervezhetőek, míg a gélesedés időtartama a tervezett alkalmazáshoz igazítható.
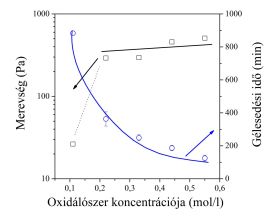
5. ábra Gélesedési idő (○) és a keletkező gélek merevsége (■) a polimer oldat összetételének függvényében
Vízoldható hatóanyag-molekulákat zártam a hidrogélbe a gélesedés során, és az így előállított géleket redukálószert tartalmazó, illetve nem tartalmazó vizes oldatba helyeztem. Redukálószer hiányában mindössze a gélbe zárt hatóanyag 20%-a oldódott ki a gélből a mérés időtartama alatt (6. ábra). Redukálószer hatására gyakorlatilag a teljes hatóanyag-mennyiség kioldódott rövid idő alatt. Eredményeim bizonyítják, hogy a redox környezettel szabályozható a gélből történő hatóanyag-leadás sebessége.[GY1].
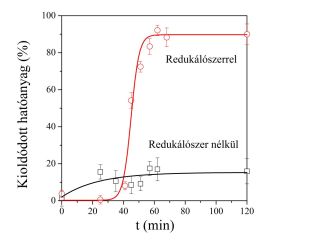
6. ábra A redukció hatása a gélekből történő hatóanyag-kioldódásra
Várható impakt, további kutatás
A Google Tudós statisztikám szerint számottevő tudományos érdeklődés fogadta eddig publikációimat, Az egyik közleményem [GY2] az European Polymer Journal (impakt faktor: 2,526) legtöbbet letöltött cikkei között szerepelt hónapokon keresztül 2013-ban.
A munkánk sikere ezen kutatási irány folytatására ösztönözte kutatócsoportunkat, együttműködésben gyógyszertechnológiai szakemberekkel. Reményeink szerint a fejlesztett polimerek alkalmasak lehetnek a szem betegségeinek az eddiginél hatékonyabb kezelésére, ugyanis a szemmel kapcsolatos problémák – a készítmények rövid tartózkodási ideje az érintett területen, a hatóanyag gyenge biohasznosulása – kiküszöbölhető egy gélesedő, erős adhéziót mutató polimer alkalmazásával [16].
Saját publikációk, hivatkozások, linkgyűjtemény
Kapcsolódó saját publikációk listája. (IF: impakt faktor, IC: független hivatkozások)
[GY1] Gyarmati B, Vajna B, Némethy Á, László K, Szilágyi A. Redox- and pH-responsive cysteamine-modified poly(aspartic acid) showing a reversible sol–gel transition. Macromol. Biosci. 2013;13(5):633-640. (IF 2012: 3,742, IC:2)
[GY2] Gyarmati B, Némethy Á, Szilágyi A. Reversible disulphide formation in polymer networks: A versatile functional group from synthesis to applications. Eur. Polym. J. 2013;49(6):1268-1286. (IF 2012: 2,562, IC:5)
[GY3] Gyarmati B, Némethy Á, Szilágyi A. Reversible response of poly(aspartic acid) hydrogels to external redox and pH stimuli. RSC Adv. 2014;4(17):8764-8771. (IF 2012 részleges: 2,562, IC:1)
[GY4] Gyarmati B, Hegyesi N, Pukánszky B, Szilágyi A. A colorimetric method for the determination of degree of chemical cross-linking in aspartic acid based polymer gels. Express Polym. Lett. 2014, Közlésre elfogadva (IF 2012: 2,294)
[GY5] Gyenes T, Torma V, Gyarmati B, Zrínyi M. Synthesis and swelling properties of novel pH-sensitive poly (aspartic acid) gels. Acta Biomater. 2008; 4(3):733-744. (IF 2012: 3,727, IC:42)
[GY6] Balogh GT, Gyarmati B, Nagy B, Molnár L, Keserű GM. Comparative evaluation of in silico pKa prediction tools on the Gold Standard dataset. QSAR Comb. Sci. 2009; 28(10):1148-1155. (IF 2012: 3,027, IC:22)
[GY7] Némethy Á, Solti K, Kiss L, Gyarmati B, Deli MA, Csányi E, Szilágyi A. pH-and temperature-responsive poly (aspartic acid)-l-poly (N-isopropylacrylamide) conetwork hydrogel. Eur. Polym. J. 2013; 49(9):2392-2403. (IF 2012: 2,562, IC:1)
[GY8] Gyarmati B, Szilágyi A. Preface for papers presented at AMSALS 2012. Period. Polytech. Chem. Eng. 2013; 58(1):47-48. (IF 2012: 0,269, IC:0)
[GY9] Horváth Z, Gyarmati B, Menyhárd A, Doshev P, Gahleitner M, Varga J, Pukánszky B. The role of solubility and critical temperatures on the efficiency of sorbitol clarifiers in polypropylene. RSC Adv. 2014; 4(38):19737-19745. (IF 2012 részleges: 2,562, IC:0)
Linkgyűjtemény
Gyógyszerek, gyógyszerformulák.
Hivatkozások listája
[1] Szilágyi A, Zrínyi M. Temperature induced phase transition of interpenetrating polymer networks composed of poly(vinyl alcohol) and copolymers of N-isopropylacrylamide with acrylamide or 2-acrylamido-2-methylpropyl-sulfonic acid. Polymer. 2005;46(23):10011-10016.
[2] Sugiura S, Szilagyi A, Sumaru K, Hattori K, Takagi T, Filipcsei G, Zrinyi M, Kanamori T. On-demand microfluidic control by micropatterned light irradiation of a photoresponsive hydrogel sheet. Lab Chip. 2009;9(2):196-198.
[3] Gyenes T, Torma V, Gyarmati B, Zrínyi M. Synthesis and swelling properties of novel pH-sensitive poly(aspartic acid) gels. Acta Biomater. 2008;4(3):733-744.
[4] Tanaka F. Classical theory of gelation. In: Tanaka F, szerk. Polymer Physics. Cambridge, UK: Cambridge University Press; 2011.
[5] Park K, Okano T. Biomedical Applications of Hydrogels Handbook. New York, USA: Springer Science+Business Media, LLC; 2010.
[6] Roy D, Cambre JN, Sumerlin BS. Future perspectives and recent advances in stimuli-responsive materials. Prog. Polym. Sci. 2010;35:278–301.
[7] Rzaev ZMO, Dinçer S, Pişkin E. Functional copolymers of N-isopropylacrylamide for bioengineering applications. Prog. Polym. Sci. 2007;32(5):534-595.
[8] Pasparakis G, Vamvakaki M. Multiresponsive polymers: nano-sized assemblies, stimuli-sensitive gels and smart surfaces. Polym. Chem. 2011;2:1234–1248.
[9] Ancla C, Lapeyre V, Gosse I, Catargi B, Ravaine V. Designed Glucose-Responsive Microgels with Selective Shrinking Behavior. Langmuir. 2011;27(20):12693-12701.
[10] Van Tomme SR, Storm G, Hennink WE. In situ gelling hydrogels for pharmaceutical and biomedical applications. Int. J. Pharm. 2008;355(1–2):1-18.
[11] Jeong B, Lee KM, Gutowska A, An YH. Thermogelling Biodegradable Copolymer Aqueous Solutions for Injectable Protein Delivery and Tissue Engineering. Biomacromolecules. 2002;3(4):865-868.
[12] Meng FH, Hennink WE, Zhong Z. Reduction-sensitive polymers and bioconjugates for biomedical applications. Biomaterials. 2009;30:2180-2198.
[13] Schafer FQ, Buettner GR. Redox environment of the cell as viewed through the redox state of the gluthathione disulfide/gluthathione couple. Free Radic. Biol. Med. 2001;30:1191–1212.
[14] Joentgen W, Müller N, Mitschker A, Schmidt H. Polyaspartic Acids. Biopolymers Online: Wiley-VCH Verlag GmbH & Co. KGaA; 2005.
[15] Bernkop-Schnürch A, Steininger S. Synthesis and characterisation of mucoadhesive thiolated polymers. Int. J. Pharm. 2000;194:239–247.
[16] Ludwig A. The use of mucoadhesive polymers in ocular drug delivery. Adv. Drug Deliver. Rev. 2005;57:1595-1639.
