 |
BMe Kutatói pályázat |

|
BME Oláh György Doktori Iskola
BME VBK, Szerves Kémia és Technológia Tanszék
Témavezető: Dr. Keglevich György
Környezetbarát szintézismódszerek kidolgozása mikrohullámú technika alkalmazásával
A kutatási téma néhány soros bemutatása
Napjainkban a vegyipar területén is egyre fontosabbá válik környezetünk és egészségünk védelme. A zöld kémia 12 alapelve szerint már a szintézisek tervezésénél olyan reakciókat célszerű választani, melyekben az alkalmazott és a keletkező anyagok a természetes környezetre nem ártalmasak; a segédanyagok használatát minimalizálni kell – ha használatuk mégis szükséges, ezek "zöldek" legyenek. A felesleges származékképzést kerülni kell, vagyis a lehető legrövidebb reakció utat célszerű választani. A szintézisek tervezésénél törekedni kell a kiindulási anyagok maximális felhasználására (nagyobb atomhatékonyságra), valamint az energiafelhasználás csökkentésére és a fenntarthatóságra. Ezen alapelvek szem előtt tartásával, munkám elsősorban a mikrohullámban (EN: microwave: MW) megvalósítható reakciók kutatásához kapcsolódik. Minden zöldkémiai megoldás hozzájárul egészségünk és környezetünk védelméhez.
A kutatóhely rövid bemutatása
A BME Szerves Kémia és Technológia Tanszékén működő, Dr. Keglevich György egyetemi tanár által vezetett Környezetbarát és Foszfororganikus Kutatócsoportban másfél évtizede foglalkoznak környezetbarát kémiával, ipari jelentőségű reakciók racionalizálásával, illetve újszerű, finomkémiai és gyógyszeripari jelentőséggel bíró foszfororganikus vegyületek előállításával. A kutatás színvonalát számos nemzetközi publikáció fémjelzi.
A kutatás történetének, tágabb kontextusának bemutatása
A mikrohullámú (MW) technika alkalmazása az elmúlt 2-3 évtizedben rohamos fejlődésen ment keresztül, miközben egyre népszerűbbé vált a kémikusok körében. A MW reaktorok első szerves kémiai alkalmazása 1986-ra tehető [1,2]. Kezdetben háztartási MW sütőkben kísérleteztek, ahol nem volt lehetőség a hőmérséklet mérésére, így a reakciók nehezen voltak reprodukálhatóak, és gyakran számoltak be robbanásszerű balesetekről is. A 2000-es évek elején megjelent, kifejezetten laboratóriumi célra készült, biztonságos, könnyen és jól szabályozható készülékek megjelenése óta a kutatás mértéke is fellendült, amit az évente megjelenő publikációk számának növekedése is jól mutat (1. ábra) [3].
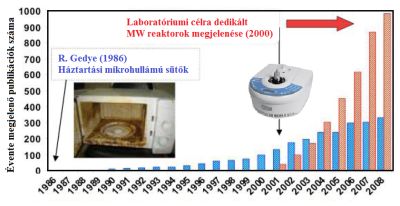
1. ábra: Publikációk számának fellendülése a dedikált MW reaktorok megjelenésétől
A mikrohullámú technika számos előnyét (ld. később) tekintve, jelentősen hozzájárul a megfogalmazott zöld kémiai elvek megvalósításához, hiszen alkalmazásával többek között elkerülhető az oldószerek használata, csökkenthető az energiafelhasználás, illetve a kémiai átalakítások hatékonyabbá tehetők.
A kutatás célja, a megválaszolandó kérdések
Doktori munkám során olyan reakciókat kutatunk, amelyek hagyományos, termikus melegítésre nem játszódnak le, ezzel szemben MW besugárzásra igen, amely ezáltal lehetővé teszi egyes veszélyes, környezetre ártalmas reagensek kiváltását, oldószer- és katalizátormentes reakciók megvalósítását.
Az egyik ilyen vizsgált reakció a foszfinsavak (1) direkt észteresítése alkoholokkal, ami hagyományos melegítéssel nem valósítható meg. A foszfinsavak észterei, vagyis a foszfinátok (2) előállítása általában foszfinsav-halogenidek (3) alkoholokkal megvalósított reakciójával történik. Ezen savkloridból kiinduló eljárásoknál azonban mindenképp probléma a hidrogén-klorid képződése, ami nem csak az atomhatékonyságot rontja, de a környezetre is ártalmas, korrozív, ráadásul a kiindulási P-halogenidek meglehetősen drágák.
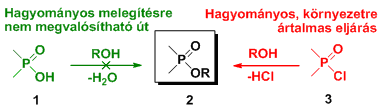
A foszfinsav-halogenidekkel megvalósított észteresítési reakciókat a fenti hátránya ellenére is széles körben alkalmazzák a szerves vegyiparban, hiszen az így kapott észterek fontos köztitermékei egyes biológiailag aktív származékok (gyógyszerek, növényvédőszerek) szintézise során. Kihívást jelentett számunkra a foszfinsavak alkoholokkal való közvetlen észteresíthetőségének vizsgálata, melyhez önkéntelenül kínálkozott a MW technika.
Kutatási munkám másik célja a MW szerves kémiai átalakításokban mutatkozó előnyeinek értelmezése, nevezetesen, hogy mi módon segíti ez a fajta hőközlés a reakciók lejátszódását. Nem ritka ugyanis, hogy a MW besugárzásnak valamiféle “mágikus” hatást tulajdonítanak, illetve napjainkban heves vita folyik a MW hatásának értelmezése körül [4].
A kérdések tisztázása érdekében, kvantumkémikusokkal együttműködve, kísérleti eredményeinket elméleti számításokkal kívántuk összevetni.
Módszerek
Doktori munkám során kísérleteinket a 2. ábrán látható MW reaktorban végeztük el.

2. ábra: CEM MW reaktor
Maga a mikrohullám (MW) az elektromágneses sugárzás infravörös és rádiófrekvencia közé eső tartományát öleli fel (3. ábra), hullámhossza 1 cm és 1 m közé esik, frekvenciája 300 MHz-től 30 GHz-ig terjed.
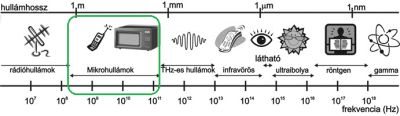
3. ábra: Mikrohullámú tartomány elhelyezkedése az elektromágneses spektrumon belül
Szemben a kevéssé hatékony és lassú tradicionális fűtési módokkal, amikor is a hőnek először a reakcióedény falán kell áthatolnia, a mikrohullámok közvetlenül találkoznak a molekulákkal és úgynevezett molekuláris fűtés valósul meg, amikor is a mikrohullámok az energiát egyenesen a reagálandó anyagokhoz juttatják (4. ábra) [5].

4. ábra: Hagyományos fűtés (![]() ) Mikrohullámú fűtés (MW)
) Mikrohullámú fűtés (MW)
A MW oszcilláló mezejének hatására a poláris molekulák igyekeznek a mezőnek megfelelően rendeződik – ezt a kölcsönhatást nevezzük dipólus forgásnak. Ezáltal gyorsan emelkedik a reakcióelegy hőmérséklete (az 5. ábrán a hőmérséklet eloszlása látható 1 perces hagyományos, illetve MW fűtés hatására [6]), és azonnali, helyhez kötött úgynevezett „superheating” következik be a reakcióelegy szegmenseiben statisztikusan eloszolva. MW besugárzás hatására az elegyben minden pillanatban máshol, akár 30-60 °C-ot is meghaladó lokális túlmelegedések lépnek fel, miközben az elegy főtömege nem hevül túl.
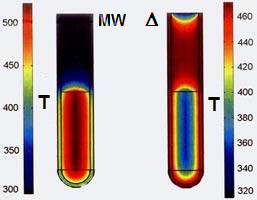
5. ábra: Hőmérséklet profil MW (balra), illetve termikus (jobbra) fűtés során
Az Arrhenius-egyenletből kiszámítható, hogy ha egy tipikus elsőrendű reakció 27 °C-on 68 napot vesz igénybe amíg eléri a 90%-os konverziót, ugyanehhez az eredményhez 227 °C-on csupán 1,6 másodpercre van szükség [7]. Ennek köszönhetően olyan átalakulások is lejátszódnak, melyek hagyományos hőközlés mellett nem valósulnának meg.
Egy ilyen, általunk talált reakció a foszfinsavak (1) direkt észteresítése, amely – szemben a karbonsav-analógokkal – hagyományos melegítésre nem játszódik le. Hogy megértsük ennek okát, magas szintű kvantumkémiai számításokat végeztettünk. Kíváncsiak voltunk, vajon termikus körülmények között miért nem reagálnak a foszfinsavak (1) alkoholokkal (hiszen a karbonsavak észteresítésének éppen ez a legegyszerűbb és legáltalánosabb módja), és szerettük volna jobban megérteni, hogy a MW miben segítheti mégis a reakció lejátszódását. A kísérleti eredményeinket elméleti számításokkal alátámasztva pedig a reakció mechanizmusának feltérképezésére is lehetőség nyílik.
Eddigi eredmények
Azt találtuk, hogy a foszfinsavak (1) és feleslegben alkalmazott (így egyúttal oldószerként is szolgáló) alkohol elegyét mikrohullámmal besugározva hatékonyan képződtek a megfelelő foszfinátok (2). Ily módon egy új módszert (1→2) dolgoztunk ki, mely a foszfinátok gazdaságos és környezetbarát előállítását teszi lehetővé [K1,2].
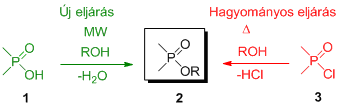
Ahhoz, hogy megértsük a karbonsavak és foszfinsavak észteresíthetősége között a különbséget, kvantumkémiai számításokat végeztettünk. A 6. ábrán ennek eredménye látható, vagyis, hogy míg a karbonsavak direkt észteresítése kismértékű energianyereséggel jár, a foszfinsavak észteresítése nem jár energianyereséggel, és a leküzdendő aktiválási “energiahegy” is nagy, így termikus körülmények között nem is várható reakció.
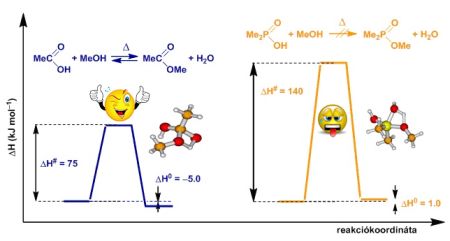
6. ábra: Karbonsavak és foszfinsavak direkt észteresítésének tipikus energiadiagramja
Az, hogy a reakció MW besugárzás hatására mégis lejátszódik, a statisztikusan, minden pillanatban máshol kialakuló lokális túlmelegedések eredménye. Ennek igazolására termikus összehasonlító kísérleteket végeztünk bombacsőben, a MW reakciókkal azonos körülmények között (azonos méret, hőmérséklet, nyomás és keverés). A termikus és a MW reakciók összehasonlítását az 1. diagramon szemléltetem, mely jól mutatja a mikrohullám szerepét a direkt észteresítések során.
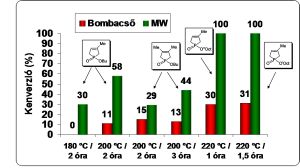
1. diagram: Hagyományos és MW fűtés összehasonlítása
A direkt észteresítésben elért eredményeink arra ösztönöztek, hogy egyes foszfinsavak (1) direkt amidálását is megkíséreljük hasonló módon. A reakció során azonban azt tapasztaltuk, hogy az amidálás nem játszódik le teljesen, MW körülmények között is legfeljebb csak 30% körüli konverziót sikerült elérnünk. Hogy megtudjuk a két reakció különbségének okát, ismét kvantumkémiai (B3LYP/6-31++G(d,p)) számításokat végeztettünk, melyek alapján elmondható, hogy míg a direkt észteresítések során a kinetikai kontroll érvényesül, a direkt amidálás termodinamikai okok miatt nem játszódik le rendesen [K9]. A direkt észteresítés és amidálás kísérleti tapasztalatait összevetve a kvantumkémiai számítások eredményeivel, általános érvényű következtetéseket vontunk le a MW szerves kémiai szintézisekben való hasznosíthatóságára, illetve korlátaira vonatkozóan [K10].
Tapasztalataink szerint nem történik semmiféle “misztikus” jelenség a MW által gyorsított, vagy lehetővé tett reakciók lejátszódásakor. Csupán arról van szó, hogy a molekulák súrlódásából származó “extra” energia (amit lokális túlmelegedésekként észlelünk), egy magasabb energiagáton is képes átlendíteni a reakciót.

7. ábra: Mikrohullámú kémia: mítosz vagy valóság? [4]
Várható impakt, további kutatás
Az előállított új vegyületek potenciális bioaktivitásuk mellett értékes intermedierek további új foszfor-heterociklusok szintéziséhez.
Az észteresítések mintájára további, hagyományos körülmények között nem megvalósítható reakciókat is vizsgálni kívánunk.
Láthattuk a MW besugárzás előnyeit, de a technika korlátairól sem szabad megfeledkeznünk, melyek közül a méretnövelhetőség talán a legnagyobb megoldandó kérdés. Erre a folyamatos üzemű MW technikák kidolgozása lehet a legkézenfekvőbb megoldás, melyek során kritérium, hogy a reakcióelegy ne legyen túl heterogén, illetve viszkózus. Az általunk vizsgált reakciók megvalósíthatónak tűnnek folytonos üzemű MW reaktorban is. Abban a szerencsés helyzetben vagyunk, hogy Tanszékünkön rendelkezésre áll ilyen, folytonos üzemű MW reaktor (sematikus vázlata a 8. ábrán látható), így a méretnövelhetőség modellezésére is lehetőségünk van.
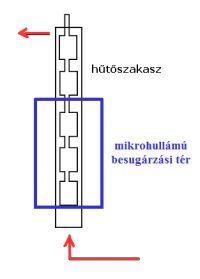
8. ábra: Folytonos üzemű MW reaktor vázlata
Saját publikációk, hivatkozások, linkgyűjtemény
Kapcsolódó saját publikációk listája:
[K1] Kiss, N. Zs.; Ludányi, K.; Drahos, L.; Keglevich, G., Synthetic Commun 2009, 39, 2392-2404. old.
[K2] Keglevich G., Bálint E., Kiss N. Zs., Jablonkai E., Hegedűs L., Grün A., Greiner I., Curr Org Chem 2011, 15, 1802-1810. old.
[K3] Keglevich, G.; Kiss, N. Zs.; Balint E.; Jablonkai E.; Grün A.; Milen M.; Frigyes D.; Greiner I., Phosphorus, Sulfur, 2011, 186, 802-803. old.
[K4] Keglevich, G.; Grün A.; Bálint E.; Kiss, N. Zs.; Kovács, R.; Greiner, I.; Molnár I.; Blastik, Zs.; Tóth, V. R.; Fehérvári, A.; Csontos, I., Phosphorus, Sulfur, 2011, 186, 613-620. old.
[K5] Keglevich, G.; Kiss, N. Zs.; Menyhárd G. K.; Fehérvári A.; Csontos I., Heteroatom Chem 2012, 23, 171-178. old.
[K6] Kiss, N. Zs.; Kaszás A.; Drahos, L.; Mucsi, Z.; Keglevich, G., Tetrahedron Lett. 2012, 53, 207–209. old.
[K7] Keglevich, G.; Kiss, N. Zs.; Mucsi, Z.; Körtvélyesi, T., Org. Biomol. Chem. 2012, 10, 2011-2018. old.
[K8] Keglevich, G.; Grün, A.; Bálint, E.; Kiss, N. Zs.; Jablonkai, E., Curr. Org. Chem. 2013, 17, 545-554. old.
[K9] Keglevich, G.; Kiss, N. Zs.; Körtvélyesi, T., Heteroatom Chem. 2013, nyomdában
[K10] Keglevich, G.; Kiss, N. Zs.; Drahos, L.; Körtvélyesi, T., Tetrahedron Lett. 2013, 54, 466-469. old.
[K11] Kiss, N. Zs.; Simon, A.; Drahos, L.; Huben, K.; Jankowski, S.; Keglevich, G. Synthesis, 2013, 45, 199-204. old.
[K12] Kiss, N. Zs.; Böttger, É. V.; Drahos, L.; Keglevich, G., Heteroatom Chem, 2013, 24, 283-288. old.
[K13] Keglevich, G.; Kiss, N. Zs.; Körtvélyesi, T.; Mucsi Z., Phosphorus, Sulfur 2013, 188, 29-32. old.
Linkgyűjtemény:
Referenciák:
[1] R. J. Giuerre, T. L. Bray, S. M. Duncan., Tetrahedron Lett. 1986, 27, 4945.
[2] R. Gedye, F. Smith, K. Westway, H. Ali, J. Rousell., Tetraherdron Lett. 1986, 27, 279.
[3] P. Lidstörm, J. Tinerney, B. Wathey, J. Westman., Tetrahedron 2001, 57, 9225.
[4] C. O. Kappe, B. Pieber, D. Dallinger., Angew. Chem. 2013, 52, 1088.
[5] L. B. Hayes., Microwave Synthesis Chemistry at the Speed of Light, CEM Publishing, USA, 2002, 11-25, 97-145. old.
[6] C. O. Kappe., Angew. Chem. Int. Ed., 2004, 43, 6250-628
[7] D. R. Baghurst, D. M. P. Mingos. Chem. Soc. Rev., 1991, 20, 1-47.
