 |
BMe Kutatói pályázat |

|
BME, Oláh György Doktori Iskola
BME VBK, Szerves Kémia és Technológia Tanszék
Témavezető: Dr. Keglevich György és Dr. Fogassy Elemér
Újszerű platina-katalizátorok szintézise és alkalmazása enantioszelektív hidroformilezési reakciókban
A kutatási téma néhány soros bemutatása
Kutatómunkám során újszerű platina-katalizátorok szintézisével foglalkozom, amelyeket a gyógyszeriparban is alkalmazható enantioszelektív hidroformilezési reakciókban lehet használni. Munkám során számos öt- és hattagú foszfortartalmú heterociklus enantiomerjeinek előállítását is kidolgoztam, amely kulcslépés volt a katalizátorok szintéziséhez.
A kutatóhely rövid bemutatása
A BME Szerves Kémia és Technológia Tanszékén a foszforkémiai kutatások, illetve az enantiomerek reszolválással történő előállítása nagy múltra tekint vissza. A két kutatócsoport együttműködése azzal a céllal kezdődött, hogy olyan foszforvegyületeket állítsanak elő enantiomertiszta formában, amelyek potenciális biológiai aktivitással rendelkeznek, illetve kiindulási anyagok katalizátorok szintéziséhez. Kutatócsoportunk szorosan együttműködik BME, a PTE, valamint az MTA TTK csoportjaival is a vegyületek abszolút konfigurációjának meghatározása, valamint az előállított katalizátorok tesztelése céljából.
A kutatás történetének, tágabb kontextusának bemutatása
A kémiában kiemelt vegyületcsoportot alkotnak a királis vegyületek, amelyek nem hozhatóak fedésbe tükörképükkel. Ha az egyik tükörképi izomerről beszélünk, akkor az enantiomer kifejezést használjuk, melyeket (R) - (S) jelöléssel különböztetjük meg egymástól. Az egymással kép-tükörkép viszonyban álló molekulák minden kémiai és fizikai tulajdonsága megegyezik, emiatt elválasztásuk nagy kihívást jelent.
A kiralitás nemcsak bizonyos molekulákra jellemző egyedi sajátság, hiszen a természetben is találkozhatunk királis objektumokkal. Elég csak arra gondolni, hogy a bal és jobb kezünk sem hozható fedésbe egymással (1. ábra).
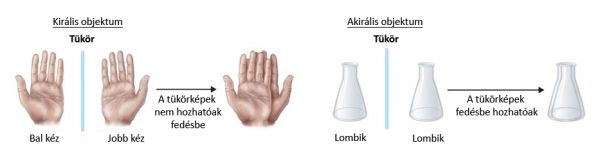
1. ábra: Királis és akirális objektumok
A szervezetbe bekerülő királis molekulák különböző enantiomerjei eltérő hatást válthatnak ki a szintén királis receptorokhoz kapcsolódva. Ezt remekül példázza, hogy az (R)-aszparagin édes ízű, míg az (S)-aszparagin íztelen.
A Contergan-botrány hívta fel a gyógyszerkutatók figyelmét arra, hogy a gyógyszermolekulák esetében is előfordulhat, hogy csak az egyik enantiomer hatásos, míg a másik hatástalan, esetleg toxikus. A Contergan néven forgalmazott Thalidomide nevű hatóanyagot a két enantiomer 1:1 arányú keverékeként, azaz racém formában hozták forgalomba, azonban csak később derült ki, hogy az egyik enantiomer volt felelős a nyugtató hatásért, míg a másik magzatkárosodást okozott (2. ábra). Ez az esemény megváltoztatta a gyógyszerkutatást, hiszen ezután kötelezővé tették, hogy minden hatóanyag engedélyeztetése előtt mindkét enantiomert elő kell állítani, és hatásukat külön kell vizsgálni. Ezek a példák jól szemléltetik, hogy az enantiomerek előállítása a gyógyszeripar érdeklődésének is a középpontjában áll.
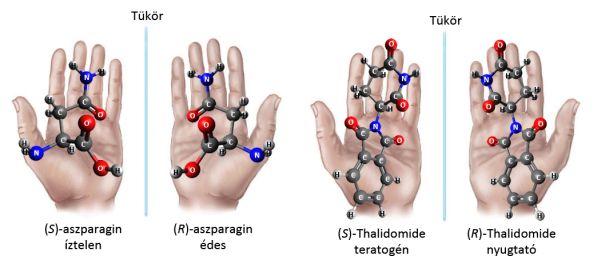
2. ábra: Az aszparagin és a Thalidomide enantiomerjeinek eltérő hatása
A kutatás célja, a megválaszolandó kérdések
A szerves foszforvegyületek kiemelten fontos szerepet töltenek be az élő szervezetekben, és a szintetikus szerves kémiában [1]. Számos biológiailag aktív foszforvegyület ismert, emellett királis foszforvegyületek átmenetifém-komplexeit alkalmazzák katalizátorként enantioszelektív hidrogénezési és hidroformilezési reakciókban [2-4]. Enantioszelektív hidroformilezési lépés alkalmazható az Ibuprofen, Naproxen és Ketoprofen nem szteroid-típusú gyulladáscsökkentők szintézisében, amely szintézisút közvetlenül a gyógyszermolekula kívánt enantiomerjét szolgáltatja, így eleget téve a zöldkémia számos alapelvének [5].
A kutatómunka során célul tűztük ki olyan foszforvegyületek enantiomerjeinek előállítását, amelyek potenciális biológiai aktivitással rendelkeznek. Célunk volt továbbá olyan enantioszelektív hidroformilezésben alkalmazható katalizátorok előállítása is, amelyeknek akár közvetlenül gyógyszeripari felhasználása is lehet (3. ábra).
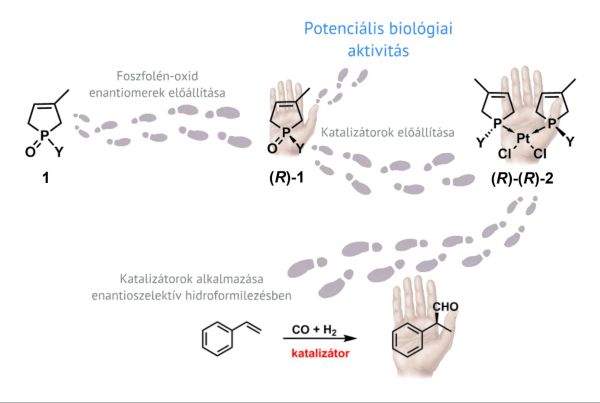
3. ábra: A kutatás célkitűzései
Kutatásunk középpontjában a foszfor-heterociklusos vegyületek, elsősorban foszfolén-oxidok (1) álltak. Ezeknek a vegyületeknek a halogénezett származékáról már kimutatták, hogy racém formában rákellenes hatásúak, azonban az egyes enantiomereket külön még nem vizsgálták [6]. Így megvalósítottuk a foszfolén-oxidok reszolválását, amely kulcslépés lehet a rákellenes hatású származékok enantiomerjeinek előállításához.
Célunk volt továbbá, hogy az előállított foszfolén-oxid enantiomerekből [(R)-1] optikailag aktív platina-komplexeket [(R)-(R)-2] állítsunk elő és teszteljük enantioszelektív hidroformilezési reakciókban. Ezekben a reakciókban királis foszfinok ródium-, illetve platina-komplexei alkalmazhatóak katalizátorként. A gazdasági világválság előtt két nemesfém ára közötti több mint ötszörös különbség indokolta a platina-alapú katalizátorokkal kapcsolatos kutatásokat (4. ábra).
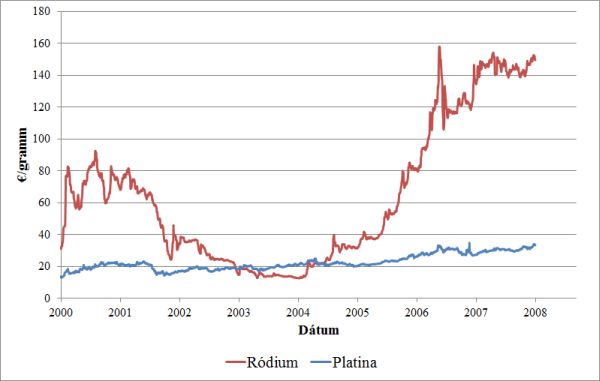
4. ábra: A ródium és platina világpiaci árának változása
Az iparban elsősorban kétfogú foszfin ligandumokat alkalmaznak, amelyekben királis információt a váz hordoz, nem a foszforatom [4,7]. Az elmúlt években megjelent összefoglaló közlemény rámutatott az egyfogú foszfin ligandumokat tartalmazó katalizátorok előnyös szelektivitására bizonyos reakciókban [8]. Így kutatásaink során arra is kerestük a választ, hogy a foszfolének, mint egyfogú foszfor aszimmetriacentrumot tartalmazó ligandumok milyen eredményességgel alkalmazhatóak hidroformilezésben, ugyanis ezt korábban még nem tanulmányozták az irodalomban.
Módszerek
A vegyületek előállítását modern preparatív szerves kémiai módszerekkel végeztük. Az anyagok tisztaságát vékonyréteg-kromatográfiával ellenőriztük. A katalitikus reakciókat autoklávban megadott nyomáson és hőmérsékleten hajtottuk végre. Az előállított vegyületek szerkezetét mágneses magrezonancia spektroszkópiával (NMR), illetve nagy felbontású tömegspektrometriával azonosítottuk.
Az előállított foszfolén-oxid enantiomerek [(R)-1] enantiomertisztaságát, valamint a katalitikus reakciók után az egyes termékek arányát gáz-, valamint folyadékkromatográfiával határoztuk meg királis állófázis alkalmazásával. A kromatográfia során a mintát egy állófázison áramoltatjuk át gáz, vagy folyadék mozgófázissal. A különböző komponensek eltérő kölcsönhatásokat alakítanak ki az állófázissal, így más időben hagyják el azt. Királis állófázist alkalmazva a különböző enantiomerek is elválaszthatóak, így meghatározható az enantiomertisztaság [9].
Az előállított foszfolén-oxid enantiomerek abszolút konfigurációját egykristály röntgendiffrakcióval és CD spektroszkópiával határoztuk meg. Az egykristály röntgendiffrakciós felvétel során röntgensugárzással bombáznak egy makroszkopikus kiterjedésű egykristályt, amelyben molekulák szabályos geometriai rendben helyezkednek el. Az egykristály optikai rácsként viselkedik a ráeső röntgensugárnyalábbal, így az elhajlik és interferál az egykristályt alkotó atomok elektronfelhőjén. A detektálható ún. interferogram alapján meghatározható az egykristályban található molekulák három dimenziós szerkezete, enantiomerek esetében az abszolút konfiguráció is.
A CD spektroszkópia is alkalmas az enantiomerek abszolút konfigurációjának meghatározására. A módszer alapja az, hogy az enantiomerek különböző mértékben nyelik el a balra, illetve jobbra forgó cirkulárisan poláros fényt. Így az adott enantiomerre jellemző spektrum vehető fel. Az abszolút konfiguráció úgy határozható meg, hogy ezt a mért CD spektrumot összehasonlítjuk kvantumkémiai számításokkal kapott spektrummal, vagy más ismert abszolút konfigurációjú származékok mért spektrumaival [10].
Eddigi eredmények
A kutatócsoportban az elmúlt években eredményes reszolválási eljárást dolgoztak ki számos foszfolén-oxid enantiomer [(R)-1] előállítására, de bizonyos alkil-szubsztituált foszfolén-oxidok esetében az enantiomertisztaság alacsony volt [11, B2].
Kutatómunkám során ezért elsősorban alkil-szubsztituált foszfolén-oxidok [(R)-1d-f] reszolválására dolgoztam ki eljárásokat, és minden esetben sikerült magas, 90% feletti enantiomertisztaságot elérni [B3, B6, B7]. Az alkil-foszfolén-oxidok [(R)-1d-f] reszolválása során az jelentette a legnagyobb kihívást, hogy az alkil-csoportok csak gyenge másodrendű kölcsönhatásokat tudnak kialakítani a reszolválóágenssel, ami rontja a reszolválás eredményességét. Ezért különösen fontos a reakciókörülmények optimálása (reszolválószer anyagi minősége és mennyisége, oldószer anyagi minősége és mennyisége, kristályosítási idő), amihez a kémiai intuíció és a szisztematikus munka mellett nagy szerencse is kell. Emellett részletesen vizsgáltam számos hattagú foszfor aszimmetriacentrumot tartalmazó vegyület (3-5) reszolválását is, és ezeknek a vegyületeknek az enantiomerjeit is elsőként állítottam elő (5. ábra) [B5, B10].
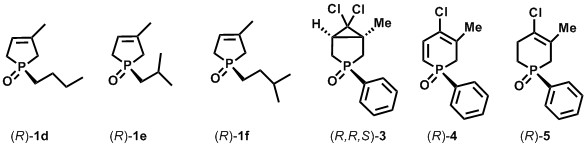
5. ábra: Az előállított öt- és hattagú foszfor heterociklusok enantiomerjei
Számos alkil-foszfolén-oxidot [(R)-1d-f] kutatómunkám során sikerült először enantiomertiszta formában előállítani, így ezek abszolút konfigurációját CD spektroszkópiával és egykristály röntgendiffrakcióval is meghatároztuk. A röntgendiffrakciós vizsgálatok során felderítettük a foszfolén-oxid és a reszolválószer között kialakuló másodrendű kölcsönhatásokat (6. ábra).
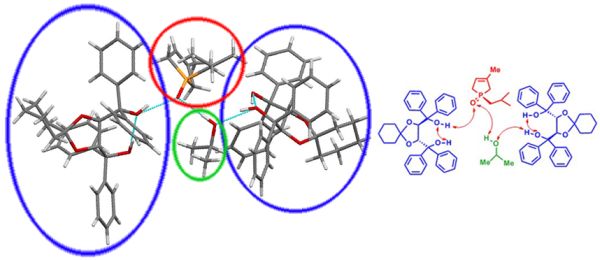
6. ábra: Az izobutil-foszfolén-oxid [(R)-1e] és a reszolválószer között kialakuló másodrendű kölcsönhatások
Az előállított foszfolén-oxid enantiomerekből [(R)-1] újszerű optikailag aktív platina- katalizátorokat [(R)-(R)-2] állítottunk elő (7. ábra). Ezek a vegyületek [(R)-(R)-2] azért újszerűek, mert - ellentétben az irodalomban található katalizátorokkal - a szintetizált platina-komplexekben a ligandum egyfogú, és az aszimmetriacentrum közvetlenül a foszforatom, nem pedig a váz egyik atomja. Így közvetlenül vizsgálni tudtuk, hogy a foszfor aszimmetriacentrumot tartalmazó foszfolének platina-komplexei alkalmas katalizátorok-e enantioszelektív hidroformilezésben. Emellett számos alkil-szubsztituenst tartalmazó származékot [(R)-(R)-2b-f] is szintetizáltunk, hogy az aszimmetrikus hidroformilezésben az alkil-láncok hatását összehasonlítsuk a fenil-csoporttal, mert az irodalomban döntően csak fenil-csoportokat tartalmazó katalizátorokat találunk [4].
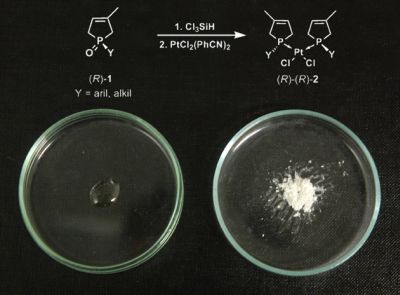
7. ábra: A katalizátorok [(R)-(R)-2] szintézise
Az előállított katalizátorokat [(R)-(R)-2] sztirol (6) hidroformilezési reakciójában teszteltük (8. ábra), amely reakció az Ibuprofen, Naproxen, Ketoprofen nem szteroid típusú gyulladáscsökkentők előállításának modellreakciója . A reakció során a sztirol (6) katalizátor jelenlétében reagál szén-monoxiddal és hidrogénnel, így termékként a 2-fenilpropanal (7), ennek regioizomerje a 3-fenilpropanal (8), valamint melléktermékként az etilbenzol (9) képződhet. A 2-fenilpropanalban (7) egy aszimmetriacentrum is található, így ennek a vegyületnek mindkét enantiomerje képződhet. Királis katalizátorokat alkalmazva azonban elérhető, hogy a 2-fenilpropanal (7) egyik enantiomerje keletkezzen feleslegben, vagy kizárólag csak az egyik enantiomer legyen a termék.
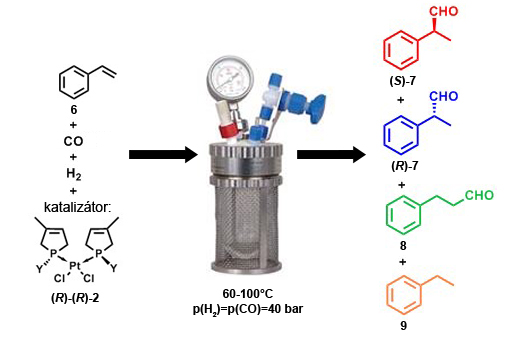
8. ábra: Sztirol (6) hidroformilezése
A katalizátor szelektivitása döntően befolyásolja, hogy melyik termék képződik. Megkülönböztetünk kemo-, regio- és enantioszelektivitást. Mivel célunk a 2-fenilpropanal egyik enantiomerjének [(S)-7] előállítása, így a katalizátor minél magasabb kemo-, regio- és enantioszelektivitása az előnyös.
Az elért eredmények alapján elmondható, hogy az egyfogú foszfolén-ligandumot tartalmazó platina-komplexek [(R)-(R)-2] eredményesen alkalmazhatóak katalizátorként sztirol (6) enantioszelektív hidroformilezési reakciójában magas kemo- és regioszelektivitással (83-92% és 64-86%). Megfigyeltük továbbá, hogy a kizárólag csak foszfor aszimmetriacentrumot tartalmazó foszfolén-ligandumokat alkalmazva, a kapott enantioszelektivitás értékek alacsonyak (3-29%) voltak (9. ábra). Részletesen vizsgálva a foszfolénhez kapcsolódó szubsztituensek szerepét azonban arra a következtetésre jutottunk, hogy a fenil-csoportok cseréje alkil-csoportokra, a regio- és enantioszelektivitás növekedését eredményezte (9. ábra a és b-f oszlop). Emellett azt is felismertük, hogy az alkil-lánc hossza és elágazása, valamint az enantioszelektivitás között tendencia van [12, B3, B6].
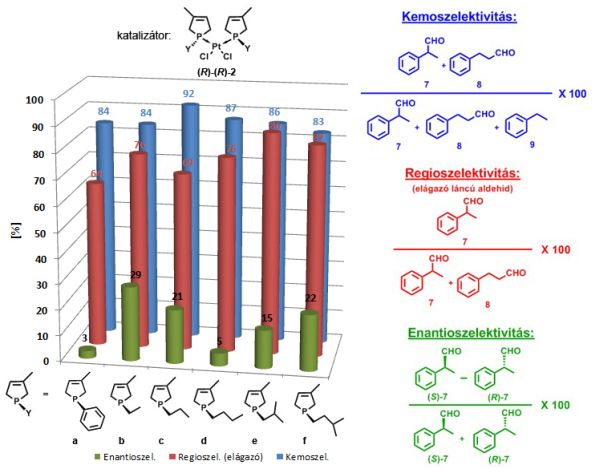
9. ábra: A foszfolén-platina komplexekkel [(R)-(R)-2] kapott katalitikus eredmények
Várható impakt, további kutatás
Kutatómunkám során számos öt- és hattagú foszfor heterociklusos vegyület (1d-f és 3-5) enantiomerjeit állítottam elő. Részletesen vizsgáltam, hogy milyen paraméterek határozzák meg a reszolválás eredményességét. Ezek az eredmények tovább bővítik ismereteinket a foszforvegyületek királis-királis felismerésével kapcsolatban, ami a jövőben lehetőséget teremthet más biológiailag aktív, illetve az iparban is alkalmazható királis foszforvegyületek reszolválásához.
Emellett újszerű foszfolén-platina komplex katalizátorokat szintetizáltunk, és sikeresen alkalmaztuk azokat enantioszelektív hidroformilezési reakcióban. Részletesen vizsgáltuk a foszfolén-gyűrűhöz kapcsolódó szubsztituensek hatását, és azt tapasztaltuk, hogy az alkil-szubsztituált származékokkal [(R)-(R)-2b-f] magasabb regio- és enantioszelektivitás érhető el, mint a megfelelő fenil-származékkal [(R)-(R)-2a].
Az eddigi kutatómunka eredményeit 6 nemzetközi folyóiratcikk formájában publikáltuk, és még 2 van előkészületben, emellett 1 könyvfejezetnek és 1 szabadalmi bejelentésnek vagyok társszerzője. Kutatómunkámat 11 hazai és nemzetközi konferencián is bemutattam szóbeli előadás, valamint poszter formájában.
A kutatás folytatásaként tervezzük hattagú foszfor-heterociklusokat, valamint további alkil-foszfoléneket tartalmazó platina-komplexek szintézisét optikailag aktív formában, és ezeket a vegyületeket is katalizátorként kívánjuk alkalmazni, hogy még mélyebben megérthessük a katalizátor szerkezete és katalitikus szelektivitása közötti összefüggést.
Saját publikációk, hivatkozások, linkgyűjtemény
Kapcsolódó saját publikációk listája.
Folyóiratcikk
[B1] Ujj, V.; Bagi, P.; Laki, A.; Fogassy, E.; Keglevich, G., Phosphorus, Sulfur, Silicon Relat. Elem. 2010, 186, 792.
[B2] Ujj, V.; Bagi, P.; Schindler, J.; Madarász, J.; Fogassy, E.; Keglevich, G., Chirality 2010, 22, 699.
[B3] Keglevich, G.; Bagi, P.; Szöllősy, Á.; Körtvélyesi, T.; Pongrácz, P.; Kollár, L.; Drahos, L.; J. Organomet. Chem. 2011, 696, 3557.
[B4] Bagi, P.; Kovács, T.; Laki, A.; Fekete A.; Fogassy, E.; Keglevich, G., Phosphorus, Sulfur, Silicon Relat. Elem. 2013, 188, 36.
[B5] Bagi, P.; Laki, A.; Keglevich, G., Heteroatom Chem. 2013, 24, 179.
[B6] Bagi, P.; Kovács, T.; Szilvási, T.; Pongrácz, P.; Kollár, L.; Drahos, L.; Fogassy, E.; Keglevich, G., J. Organomet. Chem. 2013, nyomdában
[B7] Bagi, P.; Fekete; A.; Kállay, M.; Hessz, D.; Kubinyi, M.; Holczbauer, T.; Czugler, M.; Fogassy, E.; Keglevich, G., Resolution of 1-n-butyl-, 1-n-propoxy-3-methyl-3-phosphole 1-oxides. 2013 előkészületben
[B8] Bagi, P.; Szilvási, T.; Pongrácz, P.; Kollár, L.; Drahos, L.; Fogassy, E.; Keglevich, G., Platinum(II) complexes incorporating racemic and optically active 1-aryl-3-phospholene P-ligands. 2013 előkészületben
Könyvfejezet
[B9] Keglevich, G; Bagi, P.; Bálint, E., Platinum Compounds, Production and Applications. Varrennikov, L., Yedemsky, E., szerk. Nova Science Publishers New York, 2013, 83.
Szabadalom
[B10] Bagi; P.; Fogassy, E.; Keglevich, G., Magyar Szabadalmi Bejelentés 1200228, 2012, benyújtva
11 hazai és nemzetközi konferencián szóbeli és poszter előadás
Linkgyűjtemény.
Átmenetifém-foszfin komplex (angol)
Hivatkozások listája.
[1] Quin, L. D., A guide to organophosphorus chemistry. John Wiley & Sons: New York, 2000.
[2] Brunner, H.; Zettlmeier, W., Handbook of enantioselective catalysis with transition metal compounds. VCH: Wenheim, 1993.
[3] Botteghi, C.; Marchetti, M.; Paganelli, S., szerk.; Wiley-VCH: Weinheim, 1998; Vol. 2.
[4] Kollár, L.; Keglevich, G., Chem. Rev. 2010, 110, 4257.
[5] Franke, R.; Selent, D.; Börner, A., Chem. Rev. 2012, 112, 5675.
[6] Yamada, M.; Yamashita, M.; Suyama, T.; Yamashita, J.; Asai, K.; Niimi, T.; Ozaki, N.; Fujie, M.; Maddali, K.; Nakamura, S.; Ohnishi, K., Bioorg. Med. Chem. Lett. 2010, 20, 5943.
[7] Agbossou, F.; Carpentier, J.-F.; Mortreux, A., Chem. Rev. 1995, 95, 2485.
[8] Lagasse, F.; Kagan, H. B., Chem. Pharm. Bull. 2000, 48, 315.
[9] Pokol, G,. szerk. Analitikai kémia; Typotex Kft.: Budapest, 2011.
[10] Tóth, G.; Balázs, B., Szerves vegyületek szerkezetfelderítése; Műegyetemi Kiadó: Budapest, 2005.
[11] Novák, T.; Ujj, V.; Schindler, J.; Czugler, M.; Kubinyi, M.; Mayer, Z. A.; Fogassy, E.; Keglevich, G., Tetrahedron: Asymmetry 2007, 18, 2965.
[12] Pongrácz, P.; Kollár, L.; Kerényi, A.; Kovács, V.; Ujj, V.; Keglevich, G., J. Organomet. Chem. 2011, 696, 2234.
